너텍, CGRP 억제해 편두통 치료 …급성 치료와 예방 목적 사용 가능
AZ, 릴베고스토미그+엔허투 병용 위암 1차 치료 3상 카지노 입플 승인
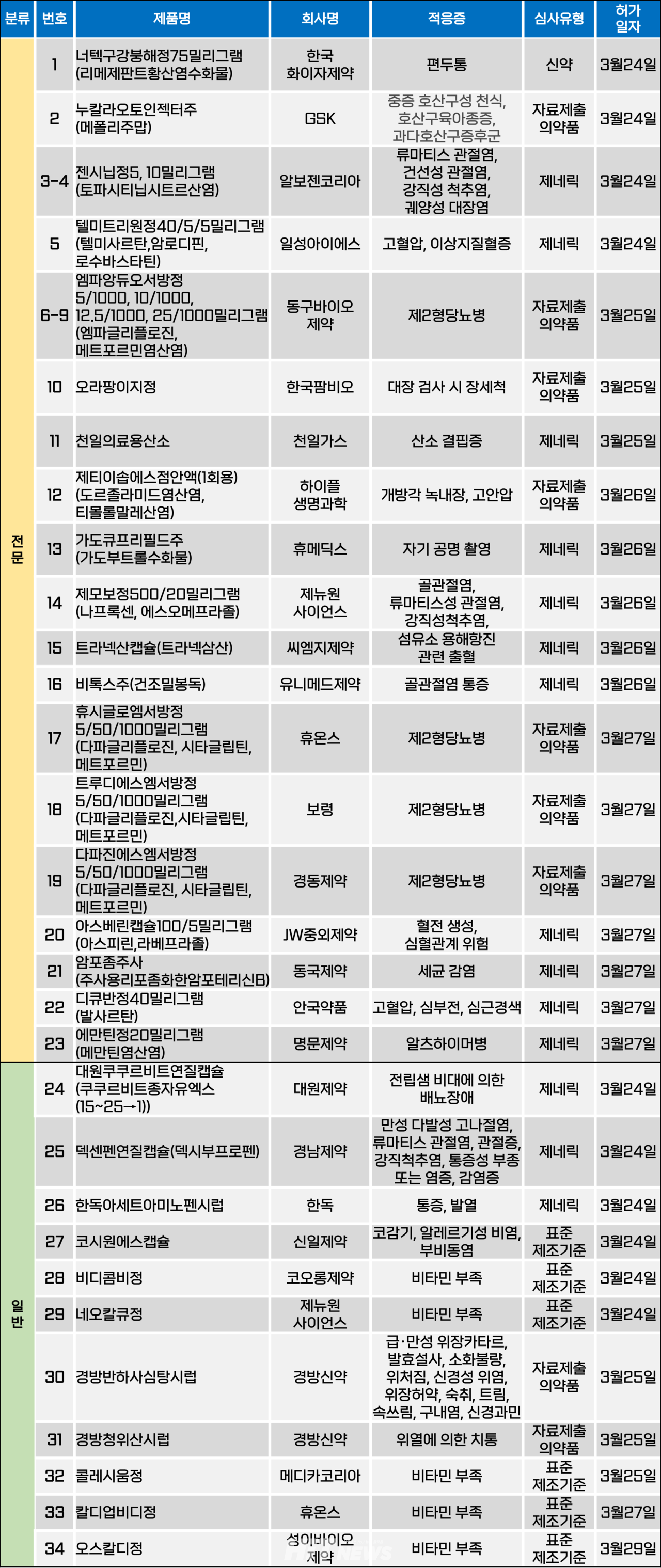
지난주(3월 24~28일) 총 34개 품목이 식품의약품안전처에서 품목허가를 받았다. 전문의약품은 23개, 일반의약품은 34개 품목이다. 이들은 편두통, 중증 호산구성 천식, 류마티스 관절염, 제2형당뇨병, 고혈압, 알츠하이머병 등 적응증으로 허가됐다.
화이자가 개발한 칼시토닌 유전자 관련 펩타이드(CGRP) 타깃 편두통 치료제 '너텍구강붕해정(성분 리메제판트)'이 지난 29일 식품의약품안전처로부터 품목허가를 획득했다.
식품의약품안전처는 너텍을 △전조증상을 수반하거나 수반하지 않는 편두통의 급성 치료 △삽화성 편두통의 예방 등 적응증으로 허가했다.
구강붕해정 제형의 너텍은 물 없이 입 안에서 녹여 복용할 수 있다. 편두통의 급성치료를 위해서는 하루 1알(75mg), 삽화성 편두통의 예방을 위해서는 격일 1알(2일 1회 75mg) 경구 투여가 권장된다.
화이자는 2022년 5월 미국 바이오기업 '바이오헤븐(Biohaven)'을 116억달러에 인수하며, 너텍의 권리를 확보한 바 있다.CGPR는 편두통의 유발하는 주요 원인으로 알려진 신경전달물질이다. 너텍은 CGRP와 수용체 간 결합을 차단해 편두통을 치료한다.
현재 국내에 허가된 CGRP 억제제는 한국애브비의 '아큅타(성분 아토제판트)'와 한국릴리 '앰겔러티(성분 갈카네주맙)'그리고 한독테바의 '아조비(성분 프레마네주맙)'가 있다. 아큅타는 CGRP 수용체를, 아조비와 앰겔러티는 CGRP 리간드를 차단한다.
두 제제 모두 편두통의 예방을 목적으로만 허가됐다는 데 공통점이 있지만, 용법용량에서는 차이가 있다. 아큅타는 1일 1회 경구용 요법으로, 앰겔러티는 월 1회 피하주사 요법(최초 2회 투여)으로, 아조비는 월 1회 또는 3개월 1회(3번 연속 투여 시) 피하주사 요법으로 허가됐다.
이 중 가장 마지막으로 출시된 아큅타는 주사제 대비 편리한 복용 방법을 내세우며, 작년 하반기부터 비급여로 상급종합병원에 입성한 바 있다. 다만, 이번 너텍의 허가로 유일한 CGRP 억제제 계열 경구용 제제라는 장점을 더 이상 내세울 수 없게 됐다.
아큅타의 급여등재와 더불어 너텍의 출시가 올해 주요 논의 사항으로 전개될 것으로 예상됨에 따라, CGRP 억제제 시장 경쟁은 더욱 심화될 것으로 전망된다.
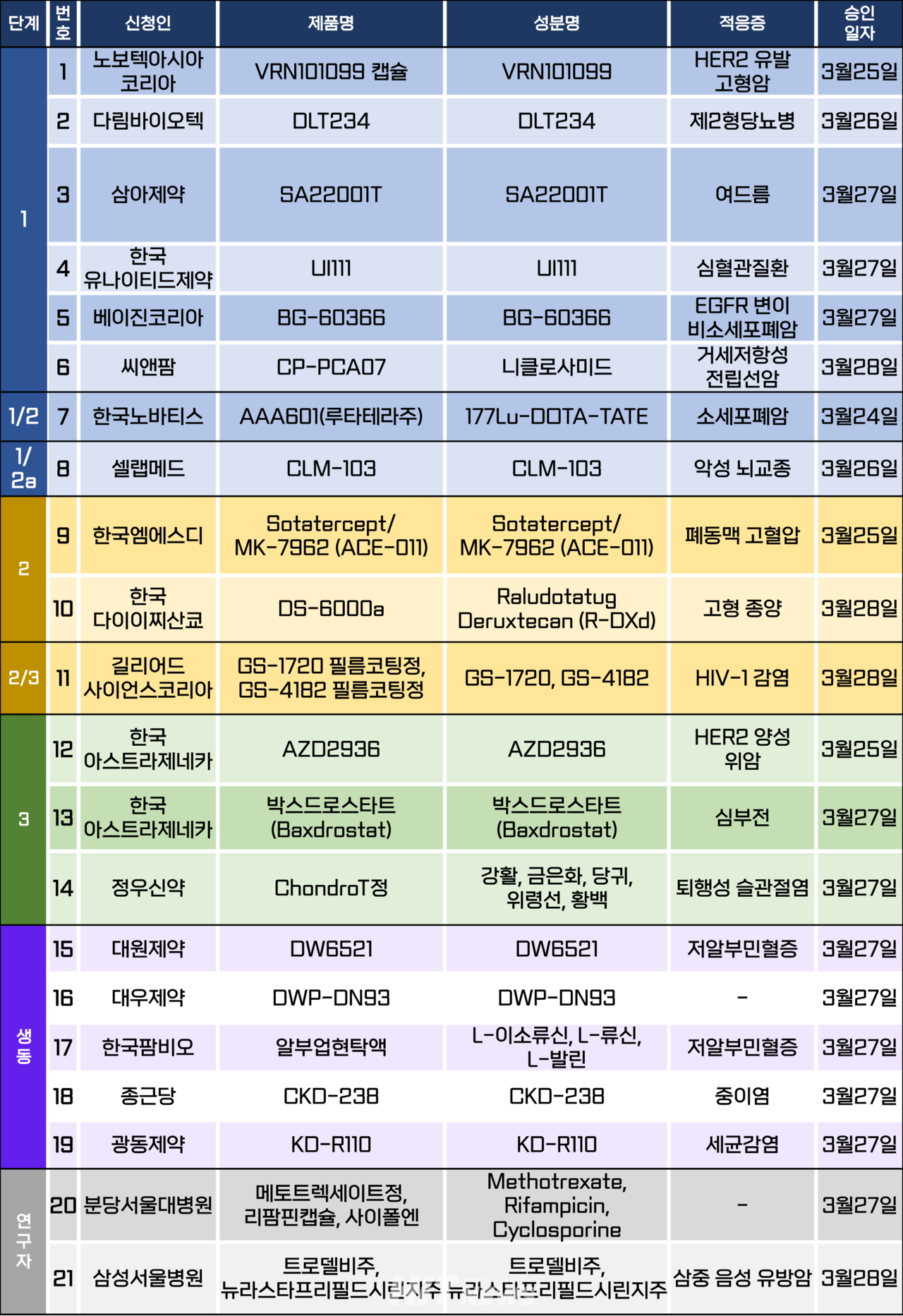
카지노 입플시험계획은 총 21건이 승인됐다. 세부적으로 △1상 6건 △1/2상 1건 △1/2a상 1건 △2상 2건 △2/3상 1건 △3상 3건 △생물학적 동등성 5건 △연구자카지노 입플 2건 등이다. 이 카지노 입플시험들은 제2형당뇨병, 페동맥 고혈압, HIV 감염, 퇴행성 슬관절염 등 질환과 비소세포폐암, 위암, 악성 뇌교종 등 암종을 대상으로 승인됐다.
PD-1/TIGIT 타깃 이중특이항체 '릴베고스토미그(Rilvegostomig, 연구명 AZD2936)'와 항체약물접합체(ADC) 엔허투(성분 트라스투주맙 데룩스테칸) 병용요법을 HER2 양성 위암 1차 치료제로 개발하기 위한 3상 카지노 입플시험이 시작된다.
아스트라제네카가 개발중인 릴베고스토미그는 항종양 T세포(Suppress antitumor T cell)의 활동을 억제하는 수용체인 PD-1과 TIGIT를 표적으로 하는 이중 특이적 인간화 항체(IgG1)이다.
한국아스트라제네카는 지난 25일 HER2 양성 위암 환자의 1 차 선택 치료로서 릴베고스토미그+엔허투+플루오로피리미딘 병용요법을 트라스투주맙(오리지널 허셉틴)+키트루다(성분 펨브롤리주맙)+항암화학요법 병용요법과 비교 평가하는 무작위배정 3상 카지노 입플시험계획(연구명 ARTEMIDE-Gastric01)을 식약처로부터 승인받았다.
이번 카지노 입플시험은 국내 60명(글로벌 840명) 환자 참여를 목표로, 2030년 12월까지 △칠곡경북대병원 △서울아산병원 △삼성서울병원 △서울대병원 △세브란스병원 △분당서울대병원 △가톨릭대 서울성모병원 등 7개 의료기관에서 진행된다.
연구진은 이번 카지노 입플시험의 1차 유효성평가변수를 독립적 맹검 평가에 의한 무진행생존기간(PFS by BICR)과 전체 생존 기간(OS)으로 설정했다. 이 중에서도 대조군 대비 위험 감소를 의미하는 '위험비(HR)'를 주요 관심 지표로 분석한다.
한편, 릴베고스토미그를 키트루다와 비교하는 카지노 입플은 이번 연구가 처음이 아니다. 회사는 종양에 PD-L1이 발현된 전이성 편평세포 비소세포폐암 환자의 1차 선택 치료로써 릴베고스토미그+백금 기반 항암화학요법과 펨브롤리주맙+백금 기반 항암화학요법을 비교하기 위한 3상 카지노 입플시험계획을 작년 8월 7일 승인받아 연구를 진행 중에 있다.
더불어 아스트라제네카는 항체약물접합체(ADC) 'Dato-DXd(성분 다토포타맙 데룩스테칸)', PD-1, CTLA-4 동시 표적 이중특이항체 'MEDI5752' 등과 릴베고스토미그의 병용요법에 대한 카지노 입플시험도 진행 중에 있다. 대상 암종은 비소세포폐암, 담도암, 위암 등이다.
