알보젠, 휴미라 시밀러 '심란디' 슬롯사이트사이트…삼성·셀트리온·LG와 경쟁 예고
신풍슬롯사이트사이트, 혈전용해제 치료 국내 환자 852명 대상 임상 진행
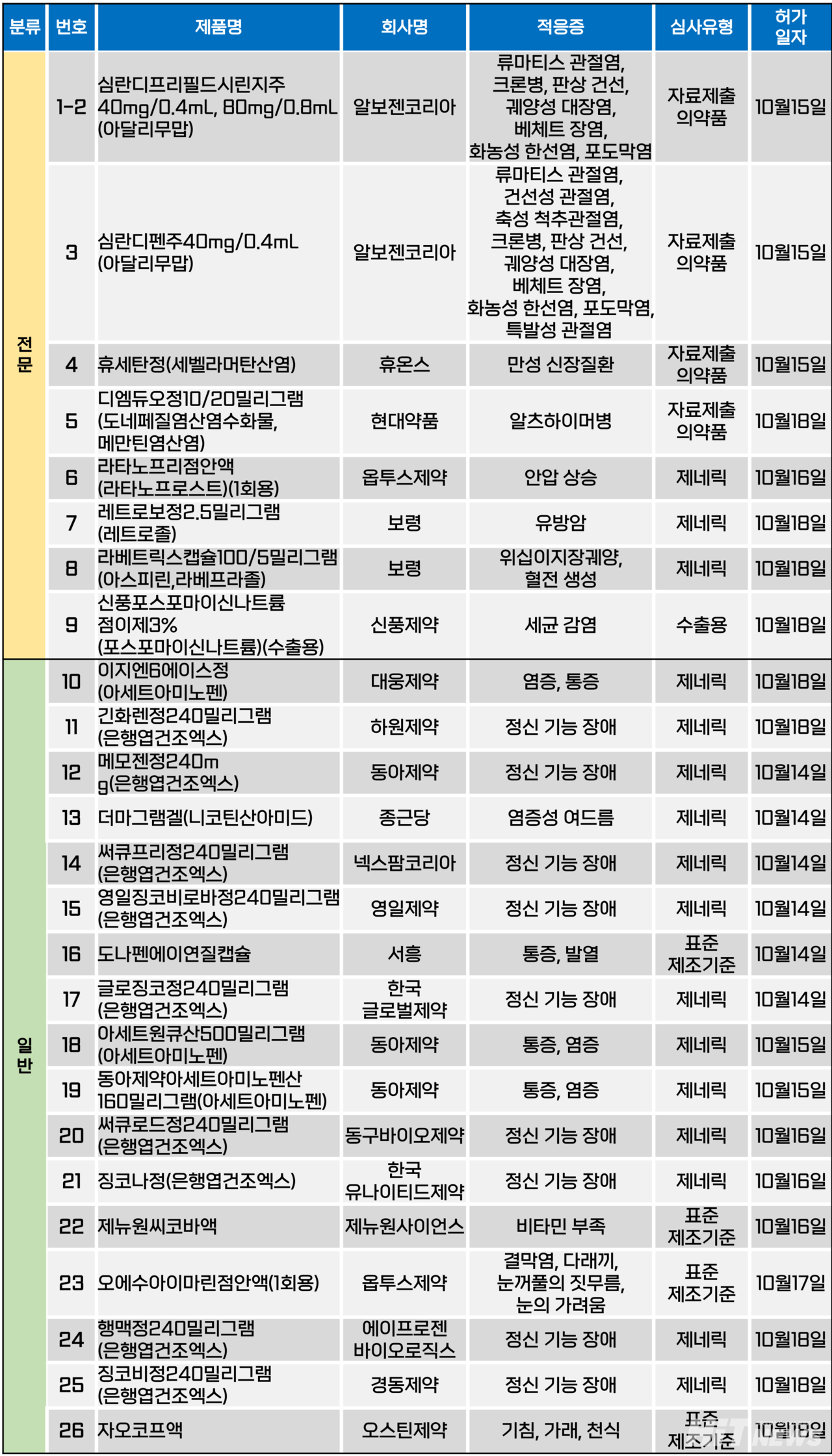
지난주(10월 14~18일) 총 26개 품목이 식품의약품안전처에서 품목슬롯사이트사이트를 받았다. 전문의약품은 9개, 일반의약품은 17개 품목이다. 이들은 류마티스 관절염, 판상 건선, 만성 신장질환, 알츠하이머병, 위·십이지장궤양 등 다양한 적응증으로 슬롯사이트사이트됐다.
자가면역치료제 '휴미라(성분 아달리무맙)'의 5번째 국내 바이오시밀러가 등장했다.
알보젠코리아는 지난 15일 '심란디펜주'40㎎/0.4㎖, '심란디프리필드시린지주'40㎎/0.4㎖ 및 80㎎/0.8㎖ 품목을 슬롯사이트사이트받았다. 슬롯사이트사이트 적응증은 제형별로차이가 있는데, 심라디펜주가 △류마티스 관절염 △건선성 관절염 △축성 척추관절염 △크론병(소아 포함) △판상 건선(소아 포함) △궤양성 대장염 △베체트 장염 △화농성 한선염 △포도막염 △소아 특발성 관절염 등을 포함하고 있으며, 프리필드시린지 제형은 건성성 관절염, 축성 척추관절염, 소아 특발성 관절염 적응증이 없다는 점을 제외하고 동일하다.
현재 국내에 슬롯사이트사이트된 휴미라 바이오시밀러는 심라디펜을 포함해 △삼성바이오에피스 '아달로체'△셀트리온 '유플라이마'△LG화학 '젤렌카'등 총 4개다.
삼성바이오에피스는 올해 초 유한양행과 코프로모션 계약 만료 후 자사 영업조직을 신설해 국내 유통하고 있으며, 셀트리온은 자회사 셀트리온슬롯사이트사이트을 통해 그리고 LG화학은 대웅슬롯사이트사이트과 함께 의약품을 공급하고 있다. 아직 알보젠이 어떤 국내 유통 방식을 선택할 지는 공개되지 않은 상태다.
한편, 애브비가 개발한 휴미라는 체내 면역 반응에 관여하는 종양괴사인자 'TNF-α'억제제로, 자가면역질환 환자에게 발생하는 염증 생성 반응을 막아 증상을 개선시킨다.
글로벌 시장조사기관에 따르면, 블록버스터 의약품 휴미라의 글로벌 매출은 2022년 기준 약 212억3700만달러(약 27조6081억원)로 추정되고 있다. 이 중 세계 최대 의약품 시장인 미국에서만 전체 매출의 87% 이상인 약 186억1900만달러(약 24조2047억원)의 매출을 기록했다.
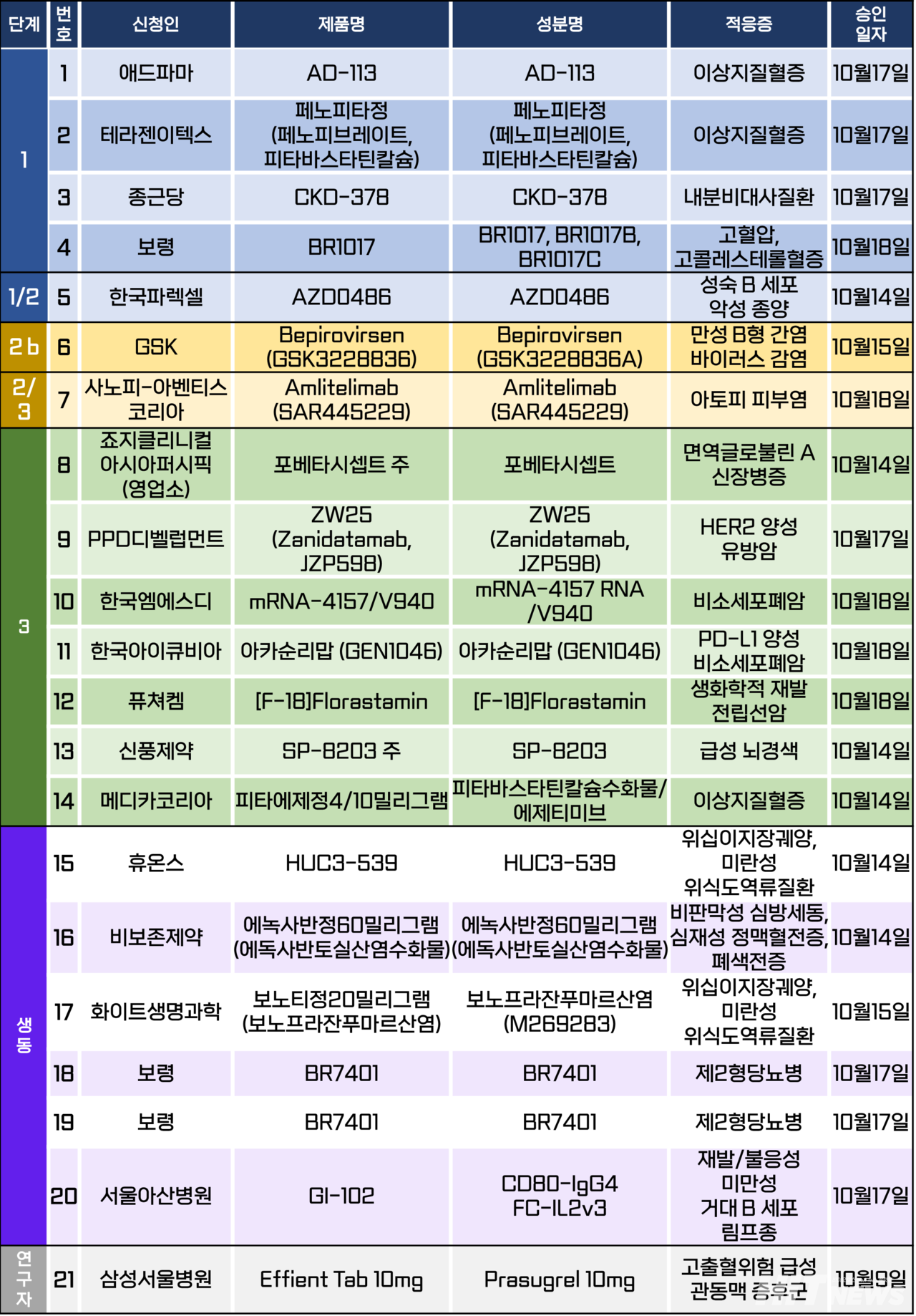
임상시험계획은 총 21건이 승인됐다. 세부적으로 △1상 4건 △1/2상 1건 △2b상 1건 △2/3상 1건 △3상 7건 △생물학적 동등성 6건 △연구자 임상 1건 등이다. 이 임상시험들은 고혈압, 이상지질혈증, 만성 B형 간염 바이러스, 면여글로불린 A 신장병증, 급성 뇌경색 등 질환과 HER2 양성 유방암, PD-L1 양성 비소세포폐암, 생화학적 재발 전립선암 등 암종을 대상으로 승인됐다.
신풍슬롯사이트사이트이 개발중인 급성 허혈성 뇌졸중(뇌경색) 신약 후보물질 '오타플리마스타트(연구명 SP-8203)'의 3상 임상시험계획이 지난 14일 승인됐다.
오타플리마스타트는 항염증 작용을 포함한 여러 신경 보호 기작을 가진 ‘퀴나졸린-2,4-다이온’ 유도체로, 신풍슬롯사이트사이트이 자체 개발중인 혁신 신약물질이다. 현재 44개국에 특허를 보유하고 있다.
뇌는 허혈 시 뉴런 및 아교세포는 흥분 독성, 산화 스트레스 및 염증 반응을 비롯한 다양한 메커니즘에 의해 손상되는데, 회사는 오타플리마스타트를 다중 세포 독성 경로를 동시 차단하는 허혈성 손상 치료제로 개발하고 있다.
이번에 승인된 3상 임상은 혈전용해제 표준 치료를 받는 급성 뇌경색 환자에서 오타플리마스타트의 유효성과 안전성을 평가하기 위한 다기관, 무작위배정, 이중눈가림, 평행, 위약대조 연구다.
국내 852명의 환자 참여를 목표로 오는 2027년 7월까지 △계명대 동산병원 △세브란스병원 △국립암센터 △서울아산병원 △삼성서울병원 △충북대병원 등 의료기관에서 진행될 예정이다.
연구진은 이번 연구의 일차유효성평가변수를 △급성 뇌경색 환자에서 혈전용해제 표준 치료 시 임상시험용의약품 첫 투여 이후 90일째에 평가한 ‘mRS(독립적 행동 지표) 0~1 비율’로 설정했다. 이차유효성평가변수는 △급성 뇌경색 환자에서 혈전용해제 표준 치료 시 임상시험용의약품 첫 투여 이후 30일째에 평가한 mRS 0~1 비율 △30일 및 90일째에 평가한 mRS 0~2 비율 △혈전용해제 표준 치료 시 90일째까지의 기저시점 대비 NIHSS의 변화량 △5일 이내에 mTICI(modified treatment in cerebral ischemia) grade로 구분된 뇌경색 부피의 증가 변화율 등이다.
한편, 오티플리마스타트는 2019년 보건복지부와 한국보건산업진흥원이 선정한 '보건의료 R&D 우수성과' 최종 30선 사례에 뽑혀 관심을 받은 바 있다.
뇌졸중의 약 80%는 허혈성 뇌졸중이지만, 표준요법인 혈전용해제를 사용하는 방법을 제외하고 치료제는 한정돼 있는 상태다. 회사 측은 오타플리마스타트 개발을 통해 표준요법 대비 환자 예후를 개선해 환자들에 추가 치료 옵션을 제시하겠다는 방침이다.
회사는 앞서 진행한 오타플리마스타트의 전기 및 후기 2상 임상시험에서 뇌경색 환자에서의 안전성과 신경학적 및 기능적 장애 개선의 결과를 도출했다고 밝혔으며, MRI 이미징 영상을 이용한 뇌경색 부피 증가에 대한 억제 효과를 입증한 바 있다.

